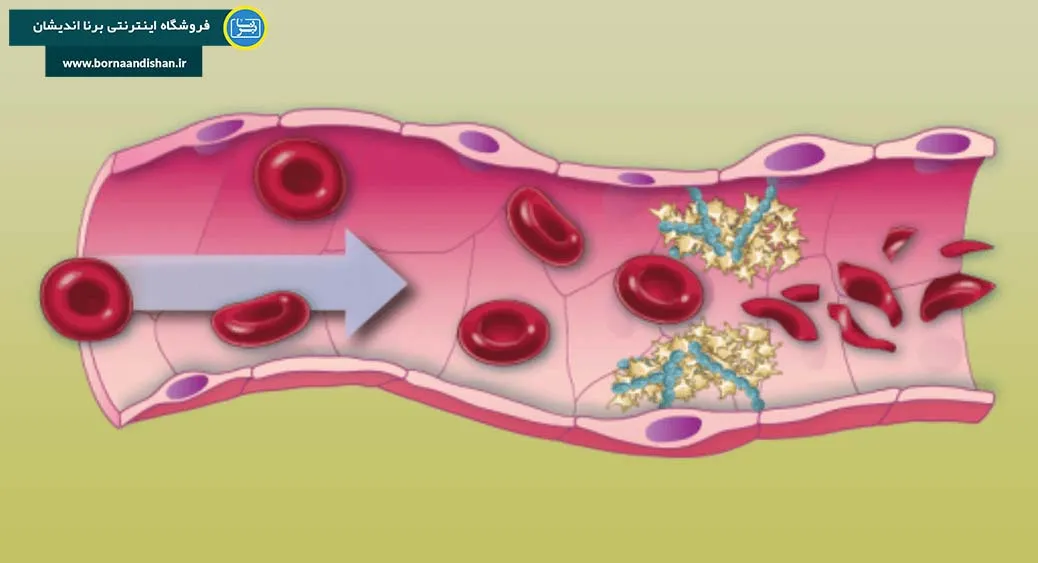
پورپورای ترومبوتیک ترومبوسیتوپنیک (Thrombotic Thrombocytopenic Purpura TTP) و سندرم همولیتیک اورمیک (Hemolytic Uremic Syndrome HUS) از جمله بیماریهای خونی مهمی هستند که بهوسیلهی کاهش تعداد پلاکتهای خون (ترومبوسیتوپنی)، کمخونی همولیتیک میکروآنژیوپاتیک و اختلالات کلیوی شناسایی میشوند. این بیماریها با ایجاد علائم مشابه، اما با مکانیسمهای متفاوت، بهویژه در تشخیص و درمان اهمیت دارند.
در این مقاله از برنا اندیشان به بررسی دقیقتر علائم، روشهای تشخیص و درمان این بیماریها خواهیم پرداخت. همچنین، پرسشهایی همچون “بیماری HUS چیست؟”، “TTP در بارداری چگونه رخ میدهد؟”، “پنتاد TTP شامل چه علائمی است؟” و “روشهای درمان TTP کدامند و چرا اهمیت دارند؟” مورد بررسی قرار خواهند گرفت.
علائم این بیماریها میتواند شامل کبودیهای غیرمعمول، خونریزیهای بیدلیل، خستگی شدید، زردی پوست و چشمها (یرقان)، کاهش ادرار و افزایش فشار خون باشد. برای تشخیص، از آزمایشهای خون و ادرار، بههمراه بررسیهای تصویربرداری و بیوپسی کلیه استفاده میشود. درمانها بسته به نوع و شدت بیماری ممکن است شامل پلاسمافرز، تجویز داروهای سرکوبکننده سیستم ایمنی و در موارد شدید، پیوند کلیه باشد.
مهمترین نکته در مواجهه با این بیماریها، تشخیص سریع و آغاز فوری درمان است تا از عوارض جدی و تهدید کننده زندگی جلوگیری شود.
پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) و سندرم همولیتیک اورمیک (HUS) چه هستند؟
پورپورای ترومبوتیک ترومبوسیتوپنیک (Thrombotic Thrombocytopenic Purpura TTP) و سندرم همولیتیک اورمیک (Hemolytic Uremic Syndrome HUS) دو بیماری خونشناختی یا هماتولوژیک مهم هستند که با کاهش تعداد پلاکتهای خون (ترومبوسیتوپنی)، کمخونی همولیتیک میکروآنژیوپاتیک (وجود گلبولهای قرمز قطعهقطعه شده یا شیستوسیت و شواهد آزمایشگاهی همولیز) و ترومبوزهای مویرگی مشخص میشوند.
این بیماریها شامل پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) و سندرم همولیتیک اورمیک (HUS) هستند، که میتوانند به صورت عارضه پیوند مغز استخوان، عارضه ناشی از برخی داروها، عفونتهای خاص، بارداری و واسکولیت نیز بروز کنند.
پیشنهاد میشود به کارگاه پزشکی بیماری زخم معده مراجعه فرمایید. پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) با تشکیل لختههای خون در عروق کوچک، که منجر به کاهش شدید پلاکتهای خون و ایجاد کمخونی همولیتیک میشود، مشخص میگردد. علائم آن شامل کبودیهای بیدلیل، خونریزیهای زیرجلدی، خستگی شدید، تب و علائم عصبی مانند سردرد و تشنج است.
سندرم همولیتیک اورمیک (HUS) نیز با کمخونی همولیتیک میکروآنژیوپاتیک و آسیب شدید به کلیهها مشخص میشود. این بیماری اغلب در کودکان به دنبال عفونتهای باکتریایی مانند E. coli بروز میکند و با علائمی مانند اسهال خونی، کاهش ادرار، فشار خون بالا و نارسایی کلیه همراه است.
تشخیص این بیماریها نیازمند آزمایشهای خونی و ادراری متعدد است و درمان آنها بسته به شدت و نوع بیماری متفاوت است، که ممکن است شامل پلاسمافرز، تجویز داروهای سرکوبکننده سیستم ایمنی و درمانهای حمایتی باشد. این دو بیماری نیازمند توجه فوری پزشکی هستند تا از بروز عوارض جدی و تهدید کننده زندگی جلوگیری شود.
تفاوت پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) و سندرم همولیتیک اورمیک (HUS)
پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) و سندرم همولیتیک اورمیک (HUS) تا پیش از این بهعنوان سندرمهای یکسانی شناخته میشدند. اما در سالهای اخیر، با پیشرفتهای علمی و درک بهتر از علت و مکانیسمهای بیماریزایی این اختلالات، مشخص شده است که این دو بیماری تفاوتهای قابل توجهی دارند.
پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) یک بیماری خونی نادر است که به علت نقص در آنزیم ADAMTS13 رخ میدهد. این نقص منجر به تشکیل لختههای خون کوچک در عروق میشود که باعث کاهش شدید پلاکتهای خون و کمخونی همولیتیک میگردد. علائم TTP شامل کبودیهای غیرمعمول، خونریزیهای زیرجلدی، خستگی شدید، تب، و علائم عصبی مانند سردرد و تشنج است. درمان TTP معمولاً شامل پلاسمافرز (تبادل پلاسما) و تجویز داروهای سرکوبکننده سیستم ایمنی است.
در مقابل، سندرم همولیتیک اورمیک (HUS) اغلب به دنبال عفونتهای باکتریایی، بهویژه باکتریهای تولید کننده توکسین شِیگا (مانند E. coli O157:H7) رخ میدهد. این توکسینها باعث آسیب به رگهای خونی کوچک کلیه شده و منجر به کمخونی همولیتیک و نارسایی کلیه میشوند. HUS بیشتر در کودکان دیده میشود و علائم آن شامل اسهال خونی، کاهش ادرار، فشار خون بالا، و نارسایی کلیه است. درمان HUS شامل مدیریت علائم، هیدراتاسیون، و در موارد شدید، دیالیز است.
در مجموع، تفاوت اصلی بین TTP و HUS در علتهای زمینهای و مکانیسمهای بیماریزایی آنها نهفته است. TTP ناشی از نقص ژنتیکی یا خودایمنی در آنزیم ADAMTS13 است، در حالی که HUS به دنبال عفونت باکتریایی و تولید توکسینهای خاص رخ میدهد. این تفاوتها نقش مهمی در تشخیص و درمان این دو بیماری دارند.
تاریخچه بیماری
پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) نخستین بار در سال ۱۹۲۴ توسط دکتر الیاس موشکوویتز توصیف شد. او علائم پنجگانهای را برای این بیماری شناسایی کرد که به عنوان پنتاد TTP شناخته میشوند. این علائم عبارتند از:
1. کمخونی همولیتیک میکروآنژیوپاتیک (Hemolytic Microangiopathic Anemia): این نوع کمخونی به دلیل تخریب گلبولهای قرمز در عروق کوچک رخ میدهد.
2. کاهش پلاکتهای خون یا ترومبوسیتوپنی (Thrombocytopenia): این کاهش شدید در تعداد پلاکتهای خون منجر به مشکلات انعقادی و خونریزی میشود.
3. نارسایی کلیوی (Kidney Disease): آسیب به کلیهها که منجر به اختلال در عملکرد آنها میگردد.
4. اختلالات مغز و اعصاب یا نورولوژیک (Neurological Disorders): این اختلالات میتواند شامل سردرد، گیجی، تشنج و سایر علائم عصبی باشد.
5. تب (Fever): افزایش دمای بدن که اغلب همراه با سایر علائم دیده میشود.
در گذشته، پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) به عنوان یک بیماری شدید و کشنده شناخته میشد. اما امروزه، به دلیل پیشرفتهای علمی و تشخیص زودرس، این بیماری به ندرت به شکل شدید خود دیده میشود. یکی از مهمترین پیشرفتها در درمان TTP، استفاده از تعویض پلاسما (پلاسمافرز) است. این روش درمانی توانسته است پیشآگهی بیماران را به طور قابلتوجهی بهبود بخشد، بهطوری که میزان مرگ و میر از ۸۵ درصد به ۱۰ درصد کاهش یافته است.
تعویض پلاسما باعث حذف عواملی میشود که به تشکیل لختههای خون منجر میشوند و آنزیم ADAMTS13 را جایگزین میکند که در بیماران TTP دچار نقص یا کاهش شده است. این روش درمانی، همراه با استفاده از داروهای سرکوبکننده سیستم ایمنی، به کنترل و مدیریت بهتر این بیماری کمک کرده است.
بنابراین، تشخیص زودرس و شروع فوری درمان، کلید موفقیت در مدیریت و بهبود بیماران مبتلا به TTP است.
علل پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) چیست؟
پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) میتواند به دو شکل ارثی و ایدیوپاتیک (ناشناخته) بروز کند. شکل ارثی آن که به سندرم آپشاو-شولمان (Upshaw-Schulman Syndrome) معروف است، و شکل ایدیوپاتیک آن که با ایجاد خودبخودی آنتیبادیهایی علیه یک متالوپروتئیناز به نام ADAMTS13 مرتبط است.
در حالت طبیعی، فاکتور فون ویلبراند (vWF) به صورت مولتیمرهای بزرگ ترشح میشود که توسط آنزیم ADAMTS13 تجزیه میشود. این تجزیه برای جلوگیری از تشکیل لختههای خونی غیر طبیعی بسیار مهم است. در بیماری TTP، به دلیل کمبود ADAMTS13 یا وجود آنتیبادیهایی که عملکرد آن را مختل میکنند، این مولتیمرهای بزرگ تجزیه نشده و منجر به تجمع پلاکتها و تشکیل لختههای خون در عروق کوچک میشوند.
با این حال، داشتن نقص در ADAMTS13 به تنهایی برای بروز بیماری کافی نیست. افرادی که به طور مادرزادی دچار کمبود ADAMTS13 هستند، فقط بهصورت دورهای دچار TTP میشوند. این موضوع نشان میدهد که علاوه بر نقص در ADAMTS13، عوامل دیگری نیز در بروز این بیماری نقش دارند که هنوز بهطور کامل شناسایی نشدهاند.
عوامل محیطی، عفونتها، استرس شدید، بارداری و برخی داروها میتوانند به عنوان محرکهای بیماری در افراد مستعد عمل کنند. برای مثال، برخی داروها مانند کینین و پلاویکس میتوانند باعث ایجاد واکنشهای ایمنی غیرطبیعی و تحریک بروز TTP شوند. همچنین، بارداری میتواند باعث تشدید علائم در زنان مبتلا به کمبود ADAMTS13 شود.
بنابراین، پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) نتیجهای از ترکیب نقص ژنتیکی یا خودایمنی در ADAMTS13 و عوامل محرک محیطی است که به تشکیل لختههای خونی غیرطبیعی منجر میشود. شناخت دقیقتر این عوامل و مکانیسمهای بیماریزا میتواند به بهبود روشهای تشخیص و درمان این بیماری کمک کند.
آزمایش تشخیص پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP)
امروزه میتوان میزان فعالیت آنزیم ADAMTS13 و وجود آنتیبادیهای مرتبط با آن را با استفاده از روشهای آزمایشگاهی دقیق تعیین کرد. این آزمایشها به تشخیص بیماری پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) کمک میکنند. با این حال، هنوز آزمایشهایی که دارای حساسیت و ویژگی کافی برای هدایت دقیق درمان باشند، به طور کامل مشخص نشدهاند.
سطح فعالیت ADAMTS13 کمتر از ۱۰ درصد به طور واضحی با پورپورای ترومبوسیتوپنیک ایمنی یا ایدیوپاتیک (ITP) مرتبط است. این نشاندهنده نقش مهم کاهش فعالیت ADAMTS13 در بیماریزایی TTP است.
نکته جالب توجه این است که پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) ایدیوپاتیک در زنان شایعتر از مردان است. این موضوع نشان میدهد که ممکن است عوامل هورمونی یا ژنتیکی نیز در بروز این بیماری نقش داشته باشند.
مراحل تشخیص
1. آزمایش خون: برای بررسی میزان پلاکتهای خون و نشانههای کمخونی همولیتیک میکروآنژیوپاتیک.
2. آزمایش فعالیت ADAMTS13: این آزمایش میزان فعالیت آنزیم ADAMTS13 را اندازهگیری میکند. سطح پایین فعالیت این آنزیم به شدت نشاندهنده TTP است.
3. آزمایش آنتیبادیها: برای شناسایی وجود آنتیبادیهایی که علیه ADAMTS13 عمل میکنند.
4. بررسیهای بالینی: پزشکان علائم و نشانههای بیماری مانند کبودیهای غیرمعمول، خونریزیهای بیدلیل، تب، و اختلالات عصبی را بررسی میکنند.
این مراحل تشخیصی به پزشکان کمک میکنند تا با دقت بیشتری TTP را تشخیص داده و درمان مناسب را شروع کنند. درمان بهموقع میتواند بهبود قابلتوجهی در پیشآگهی بیماران ایجاد کند.
TTP در بارداری و ایدز
پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) در بیماران مبتلا به عفونت HIV (و ایدز) و در زنان باردار شیوع بیشتری دارد. این افزایش شیوع نشاندهنده اهمیت ویژهای است که باید به این بیماری در این گروههای خاص داده شود.
TTP در بیماران مبتلا به HIV و ایدز
افرادی که به HIV مبتلا هستند، به دلیل ضعف سیستم ایمنی، مستعد ابتلا به TTP میشوند. عفونت HIV میتواند منجر به تولید آنتیبادیهای غیرطبیعی علیه ADAMTS13 شود که باعث کاهش فعالیت این آنزیم و افزایش خطر تشکیل لختههای خونی میشود. علاوه بر این، التهاب مزمن و اختلالات ایمنی مرتبط با HIV میتواند به تسریع بروز TTP کمک کند.
TTP در بارداری
TTP در دوران بارداری نیز نسبتاً شایعتر است، اما علت دقیق بروز آن هنوز بهطور کامل مشخص نشده است. برخلاف برخی موارد دیگر TTP، این بیماری در بارداری لزوماً با کمبود ADAMTS13 مرتبط نیست. احتمال دارد تغییرات فیزیولوژیکی و هورمونی دوران بارداری، بهویژه در سهماهه سوم، نقش مهمی در بروز این بیماری ایفا کنند. همچنین، استرس بارداری میتواند بهعنوان یک محرک برای بروز TTP در زنانی که بهطور ژنتیکی مستعد هستند، عمل کند.
اهمیت تشخیص و درمان
تشخیص سریع TTP در زنان باردار و بیماران مبتلا به HIV بسیار حیاتی است. عدم تشخیص و درمان بهموقع میتواند منجر به عوارض جدی برای مادر و جنین و همچنین تشدید علائم در بیماران HIV مثبت شود. درمان معمولاً شامل پلاسمافرز و استفاده از داروهای سرکوبکننده سیستم ایمنی است که میتواند به بهبود علائم و کاهش خطر عوارض کمک کند.
در مجموع، افزایش آگاهی درباره خطرات و علائم TTP در این گروههای خاص، و انجام بررسیهای دورهای، میتواند به تشخیص زودهنگام و مدیریت موثر این بیماری کمک کند و از عوارض جدی آن جلوگیری نماید.
پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) ناشی از دارو
TTP ناشی از دارو میتواند به علت تشکیل آنتیبادیها یا آسیب مستقیم به سلولهای اندوتلیال عروق رخ دهد. این عارضه ممکن است به دلایل مختلفی از جمله عوارض جانبی داروهای زیر به وجود آید:
داروهایی که باعث تشکیل آنتیبادیها میشوند:
- تیکلوپیدین (Ticlopidine)
- کلوپیدوگرل (Clopidogrel)
این داروها میتوانند باعث تولید آنتیبادیهایی شوند که علیه آنزیم ADAMTS13 عمل کرده و فعالیت آن را کاهش دهند. این کاهش فعالیت منجر به تشکیل لختههای خونی و بروز TTP میشود.
داروهایی که باعث آسیب مستقیم به اندوتلیوم میشوند:
- سیکلوسپورین (Cyclosporine)
- میتومایسین (Mitomycins)
- تاکرولیموس (Tacrolimus)
- کینین (Quinine)
این داروها ممکن است باعث آسیب مستقیم به سلولهای اندوتلیال عروق شوند که منجر به میکروآنژیوپاتی و تشکیل لختههای خونی کوچک میشود. اگرچه این ارتباط همیشه به وضوح مشخص نیست، اما تجربه بالینی نشان داده است که قطع یا کاهش دوز این داروها میتواند به کاهش علائم و بهبود وضعیت بیماران کمک کند.
درمان TTP ناشی از دارو
به دلیل ترس از قطع درمان مؤثر اصلی و نیز نبود گزینههای درمانی جایگزین، اغلب از تعویض پلاسما بهعنوان درمان اصلی TTP ناشی از دارو استفاده میشود. این روش درمانی میتواند به حذف آنتیبادیها و عوامل التهابی کمک کرده و بهبود سریعتری را فراهم کند.
راهکارهای مدیریتی
1. تشخیص سریع و دقیق: تشخیص به موقع TTP ناشی از دارو برای جلوگیری از عوارض جدی بسیار مهم است.
2. قطع یا تنظیم دوز دارو: در صورتی که داروی مشکوک به ایجاد TTP باشد، قطع یا تنظیم دوز آن میتواند به کاهش علائم کمک کند.
3. تعویض پلاسما: این روش درمانی بهویژه در موارد حاد و شدید میتواند بسیار موثر باشد.
4. پایش مداوم: بیماران باید به طور مداوم تحت نظر پزشک باشند تا در صورت بروز هرگونه علائم جدید، اقدامات لازم به سرعت انجام شود.
در مجموع، شناخت دقیق علل و مکانیسمهای TTP ناشی از دارو و استفاده از راهکارهای مدیریتی مناسب، میتواند به بهبود وضعیت بیماران و کاهش خطرات و عوارض ناشی از این بیماری کمک کند.
تشخیص TTP در آزمایش خون
تشخیص پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) از طریق آزمایشهای خون انجام میشود که نشاندهنده مجموعهای از تغییرات خاص در پارامترهای خونی است. این نشانهها عبارتند از:
1. افزایش میزان لاکتات دهیدروژناز (LDH): سطح بالای LDH نشاندهنده تخریب گلبولهای قرمز است که یکی از ویژگیهای اصلی TTP میباشد.
2. افزایش بیلیروبین غیرمستقیم: این افزایش نیز نتیجه همولیز (تخریب گلبولهای قرمز) است.
3. کاهش میزان هاپتوگلوبین خون: هاپتوگلوبین پروتئینی است که به هموگلوبین آزاد در خون متصل میشود. کاهش سطح آن نشاندهنده همولیز است.
4. افزایش شمار رتیکولوسیتها: به دلیل افزایش تولید گلبولهای قرمز جوان به عنوان پاسخ به همولیز، تعداد رتیکولوسیتها افزایش مییابد.
5. نتیجه منفی آزمایش آنتیگلوبولین مستقیم (Coombs Test): این نتیجه نشان میدهد که همولیز ناشی از فرآیندهای ایمنی مانند آنتیبادیهای ضد گلبولهای قرمز نیست.
بررسی گستره خون محیطی (Peripheral Blood Smear)
برای تشخیص دقیقتر، گستره خون محیطی باید از نظر وجود شیستوسیتها (گلبولهای قرمز تکهتکه شده) بررسی شود. وجود شیستوسیتها یکی از نشانگرهای کلیدی در تشخیص TTP است. علاوه بر این، به دلیل افزایش تعداد رتیکولوسیتها، معمولا پلیکرومازی (حضور گلبولهای قرمز با رنگآمیزی چندگانه) دیده میشود. همچنین، حضور گلبولهای قرمز هستهدار نیز ممکن است مشاهده شود.
خلاصه نکات تشخیصی
- افزایش LDH و بیلیروبین غیرمستقیم: نشاندهنده همولیز فعال.
- کاهش هاپتوگلوبین: تأیید تخریب گلبولهای قرمز.
- افزایش رتیکولوسیتها: پاسخ مغز استخوان به همولیز.
- نتیجه منفی Coombs Test: نشاندهنده عدم وجود آنتیبادیهای ضد گلبولهای قرمز.
- گستره خون محیطی: حضور شیستوسیتها و پلیکرومازی.
این پارامترها و نشانهها به تشخیص TTP کمک میکنند و باید توسط پزشکان متخصص برای تایید نهایی تشخیص و تعیین برنامه درمانی مورد بررسی قرار گیرند. تشخیص زودهنگام و دقیق این بیماری میتواند به بهبود پیشآگهی و کاهش عوارض جدی کمک کند.
درمان بیماری TTP چیست؟
پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) در صورت عدم تشخیص و درمان فوری میتواند کشنده باشد. بنابراین، تشخیص سریع و شروع درمان از اهمیت حیاتی برخوردار است. بیمارانی که با کاهش پلاکت خون (ترومبوسیتوپنی) به پزشک مراجعه میکنند، چه با علائم نارسایی کلیوی و چه بدون آن، باید جهت رد DIC (اختلال انعقادی منتشره در عروق) و ارزیابی علائم کمخونی همولیتیک میکروآنژیوپاتیک مورد آزمایش خون قرار گیرند.
تعویض پلاسما (Plasma Exchange)
تعویض پلاسما بهعنوان اصلیترین درمان TTP شناخته میشود. این روش به ویژه در مواردی که بیماری به دلیل وجود آنتیبادی علیه ADAMTS13 ایجاد شده باشد (TTP ایدیوپاتیک)، بسیار مؤثر است. درمان با تعویض پلاسما تا زمانی که تعداد پلاکتهای خون به سطح طبیعی بازگردد و علائم همولیز برای حداقل ۲ روز از بین برود، ادامه مییابد.
استفاده از گلوکوکورتیکوئیدها
اگرچه کارآزماییهای بالینی استفاده از گلوکوکورتیکوئیدها (کورتونها) را بهطور کامل ارزیابی نکردهاند، اما به نظر میرسد که این داروها میتوانند بهعنوان یک درمان کمکی در کنار تعویض پلاسما مفید باشند. گلوکوکورتیکوئیدها به کاهش التهاب و سرکوب پاسخ ایمنی کمک میکنند.
داروهای سرکوبکننده ایمنی
در مواردی که TTP به درمان مقاوم است یا عود میکند، از داروهای سرکوبکننده ایمنی استفاده میشود. برخی از این داروها عبارتند از:
- ریتوکسیماب (Rituximab): یک آنتیبادی مونوکلونال که به تخریب سلولهای B کمک میکند.
- وین کریستین (Vincristine): یک داروی شیمیدرمانی که سلولهای ایمنی را هدف قرار میدهد.
- سیکلوفسفامید (Cyclophosphamide): یک داروی سرکوبکننده سیستم ایمنی که برای کاهش تولید آنتیبادیها استفاده میشود.
- برداشتن طحال (Splenectomy): در موارد مقاوم به درمان، برداشتن طحال میتواند کمککننده باشد.
نرخ عود بیماری
حتی با وجود این درمانها، میزان عود TTP بالا است و بین ۲۵ تا ۴۵ درصد گزارش شده است. بیمارانی که در زمان مراجعه دچار کمبود شدید ADAMTS13 هستند، بیشتر در معرض عود بیماری قرار دارند. این امر نیازمند پیگیری مداوم و نظارت دقیق پس از درمان اولیه است تا در صورت بروز علائم مجدد، اقدامات درمانی سریعاً آغاز شود.
تشخیص سریع و شروع فوری درمان برای مدیریت TTP ضروری است. تعویض پلاسما به عنوان درمان اصلی، همراه با استفاده از گلوکوکورتیکوئیدها و داروهای سرکوبکننده ایمنی میتواند به بهبود علائم و کاهش خطرات بیماری کمک کند. با این حال، نظارت مداوم و پیگیری منظم برای جلوگیری از عود بیماری ضروری است.
علت بیماری HUS در کودکان و بالغین چیست؟
سندرم همولیتیک اورمیک (HUS) در کودکان شایعتر از بزرگسالان است، هرچند که این بیماری ممکن است در بزرگسالان نیز رخ دهد و در این صورت، معمولاً شدیدتر و کشندهتر خواهد بود.
HUS در کودکان
بیماری HUS در کودکان معمولاً پس از یک دوره اسهال، بهویژه اسهال خونی، بروز میکند. علت اصلی HUS در کودکان عفونت با باکتریهای خاصی مانند اشریشیا کولی O157:H7 و برخی دیگر از سویههای باکتریایی است. این باکتریها تولید توکسین شِیگا (Shiga toxin) میکنند که باعث آسیب به عروق کوچک کلیه و بروز HUS میشود.
علاوه بر موارد همراه با اسهال، HUS میتواند بدون علائم اسهال نیز بروز کند. این نوع HUS از نظر نحوه بروز و سیر بیماری تنوع بیشتری دارد و ممکن است به دلایل مختلفی مانند عفونتهای دیگر یا عوامل ژنتیکی رخ دهد.
HUS در بزرگسالان
سندرم همولیتیک اورمیک در بزرگسالان که به نام HUS آتیپیک (aHUS) نیز شناخته میشود، بهطور عمده به دلایل ژنتیکی رخ میدهد. این نوع HUS به دلیل نقصهای ژنتیکی در تنظیم کمپلمان سیستم ایمنی ایجاد میشود که منجر به فعالیت مزمن و غیرقابل کنترل کمپلمان میگردد.
برای تشخیص HUS آتیپیک، غربالگری برای بررسی جهش در ژنهای تنظیمکننده کمپلمان انجام میشود. این ژنها شامل فاکتور H، فاکتور I، CD46، و دیگر ژنهای مرتبط با مسیر کمپلمان هستند. نقص در این ژنها منجر به فعالیت بیش از حد کمپلمان و آسیب به عروق کوچک، بهویژه در کلیهها، میشود.
تفاوتهای HUS در کودکان و بزرگسالان
- علت بروز: در کودکان معمولاً بهدنبال عفونتهای باکتریایی ایجاد میشود، در حالیکه در بزرگسالان اغلب به دلایل ژنتیکی و نقصهای کمپلمان رخ میدهد.
- شدت بیماری: HUS در بزرگسالان معمولاً شدیدتر و با عوارض بیشتر همراه است.
- روشهای تشخیصی: در کودکان، تشخیص بیشتر بر اساس علائم بالینی و تاریخچه بیماری اسهال استوار است، در حالیکه در بزرگسالان، غربالگری ژنتیکی برای تشخیص نقصهای کمپلمان انجام میشود.
شناخت دقیق علل و مکانیسمهای بیماری HUS در کودکان و بزرگسالان، به تشخیص صحیح و درمان مؤثر این بیماری کمک میکند. در کودکان، مدیریت عفونتهای باکتریایی و پیشگیری از اسهال خونی اهمیت ویژهای دارد، در حالیکه در بزرگسالان، تشخیص و مدیریت نقصهای ژنتیکی مرتبط با سیستم کمپلمان از اهمیت بالایی برخوردار است.
علائم سندرم همولیتیک اورمیک (بیماری HUS) چیست؟
سندرم همولیتیک اورمیک (HUS) یک بیماری جدی است که با سه علامت اصلی شناخته میشود:
نارسایی حاد کلیوی (Acute Renal Failure ARF)
- این وضعیت به دلیل آسیب شدید به عروق کوچک کلیهها رخ میدهد که منجر به کاهش یا توقف عملکرد کلیهها میشود.
- علائم نارسایی کلیوی شامل کاهش ادرار، تورم در اندامها و افزایش فشار خون است.
- آزمایشهای خون نشاندهنده افزایش سطح کراتینین و اوره، و وجود پروتئین و خون در ادرار است.
کمخونی همولیتیک میکروآنژیوپاتیک
- این نوع کمخونی به دلیل تخریب گلبولهای قرمز خون در عروق کوچک اتفاق میافتد.
- علائم شامل ضعف، خستگی، رنگپریدگی، زردی پوست و چشمها (یرقان) و نفستنگی است.
- آزمایش خون نشاندهنده کاهش تعداد گلبولهای قرمز، افزایش لاکتات دهیدروژناز (LDH)، و کاهش هاپتوگلوبین است.
کاهش پلاکتهای خون یا ترومبوسیتوپنی (Thrombocytopenia)
- کاهش تعداد پلاکتها باعث مشکلات انعقادی و خونریزی میشود.
- علائم شامل کبودیهای بیدلیل، خونریزی از لثهها یا بینی، و وجود نقاط قرمز کوچک روی پوست (پتشی) است.
- آزمایش خون نشاندهنده کاهش شدید پلاکتها و افزایش زمان خونریزی است.
این سه علامت اصلی که به عنوان تریاد کلاسیک HUS شناخته میشوند، اغلب به دنبال یک عفونت باکتریایی، بهویژه باکتری اشریشیا کولی (E. coli) تولید کننده توکسین شِیگا، در کودکان بروز میکنند. در موارد دیگر، بهویژه در بزرگسالان، ممکن است به دلایل ژنتیکی یا نقصهای سیستم کمپلمان رخ دهند. تشخیص زودهنگام و شروع فوری درمان میتواند از بروز عوارض جدیتر جلوگیری کند و پیشآگهی بیمار را بهبود بخشد.
درمان سندرم همولیتیک اورمیک (بیماری HUS)
پیشنهاد میشود به پاورپوینت سندرم رت مراجعه فرمایید. درمان سندرم همولیتیک اورمیک (HUS) عمدتاً حمایتی است و هدف آن مدیریت علائم و جلوگیری از عوارض جدی است. روشهای درمانی برای دو نوع اصلی این بیماری یعنی HUS همراه با اسهال و HUS آتیپیک متفاوت است.
درمان HUS همراه با اسهال (D+ HUS)
- دیالیز: بسیاری از کودکان مبتلا به HUS همراه با اسهال (تقریباً ۴۰ درصد) نیازمند حداقل یک دوره دیالیز هستند تا عملکرد کلیهها را بهبود بخشند. دیالیز به حذف مواد زائد و سموم از خون کمک میکند که کلیههای آسیبدیده قادر به انجام آن نیستند.
- مراقبتهای حمایتی: این شامل مدیریت مایعات و الکترولیتها، کنترل فشار خون و پیشگیری از عفونتهای ثانویه است.
- پیشآگهی: میزان مرگ و میر ناشی از HUS همراه با اسهال کمتر از ۵ درصد است که نشاندهنده پیشآگهی نسبتاً خوب در این نوع بیماری است.
درمان HUS آتیپیک (aHUS)
میزان مرگ و میر: در HUS آتیپیک که با اسهال همراه نیست، میزان مرگ و میر بالاتر است و به تقریباً ۲۶ درصد میرسد.
تزریق پلاسما یا تعویض پلاسما: این روشها تاثیر قابل توجهی بر سیر کلی بیماری ندارند. بر خلاف پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP)، سطح ADAMTS13 در HUS طبیعی است، هرچند که ممکن است گاهی کاهش یابد.
درمان با اکولیزوماب (Eculizumab): اکولیزوماب، یک داروی مونوکلونال است که بر روی سیستم کمپلمان اثر میگذارد. در بیماران مبتلا به HUS آتیپیک، این دارو میتواند تعداد پلاکتهای خون را افزایش داده و عملکرد کلیه را حفظ کند. درمان با اکولیزوماب باعث مهار پروتئین کمپلمان C5 میشود که در پیشگیری از آسیبهای ناشی از فعالیت بیش از حد کمپلمان موثر است.
خلاصه درمان
- حمایت کلیوی: استفاده از دیالیز در موارد حاد نارسایی کلیه.
- مدیریت مایعات و الکترولیتها: جهت حفظ تعادل بدن و جلوگیری از عوارض.
- استفاده از داروهای خاص: مانند اکولیزوماب در HUS آتیپیک برای مهار فعالیت کمپلمان و بهبود عملکرد کلیه.
- پیشگیری و مراقبت: نظارت دقیق بر علائم و مدیریت عوارض بالقوه برای بهبود پیشآگهی.
درمان بهموقع و مناسب میتواند بهبود قابل توجهی در کیفیت زندگی بیماران مبتلا به HUS ایجاد کند و از بروز عوارض جدیتر جلوگیری نماید.
نتیجهگیری
پورپورای ترومبوتیک ترومبوسیتوپنیک (TTP) همانند یک جنگجوی نامرئی در میدان نبرد بدن انسان ظاهر میشود، آماده برای حمله به سیستم خونی و ایجاد لختههای مرگبار. اما این جنگ، یک نبرد بیپایان و غیرقابل پیروزی نیست. علم پزشکی، همچون یک قهرمان، راهحلهایی را برای مقابله با این دشمن پنهان فراهم کرده است.
درک و آگاهی
درک مکانیسمهای پیچیده TTP و شناخت دقیق علتهای آن، نخستین گام در راه مبارزه است. تشخیص زودهنگام و دقیق، همچون یک سپر دفاعی، میتواند از گسترش این بیماری جلوگیری کند و زندگی بیمار را به مسیر عادی بازگرداند.
سلاحهای درمانی
تعویض پلاسما، همچون یک نجاتبخش فوری، میتواند عوامل مضر را از بدن خارج کند و به بهبود عملکرد پلاکتها کمک کند. استفاده از داروهای سرکوبکننده ایمنی و گلوکوکورتیکوئیدها، به عنوان یاران وفادار در این مبارزه، نقش حیاتی در کنترل و مدیریت بیماری ایفا میکنند. در موارد مقاوم، ریتوکسیماب و سایر داروهای جدید همچون سلاحهای پیشرفتهای هستند که قدرت دفاعی ما را افزایش میدهند.
اهمیت پیگیری و پایداری
اما نبرد با TTP تنها با یک حمله پیروز نمیشود. پیگیری منظم و پایدار، همچون نگهبانی دائمی، برای جلوگیری از عود بیماری و حفظ سلامت بیمار ضروری است. ارتباط مستمر با تیم پزشکی و انجام آزمایشهای دورهای، همانند بررسی نقشههای جنگی، به شناسایی سریع هرگونه نشانههای عود کمک میکند.
امید و بهبودی
در پایان، پیام امیدبخش ما این است: TTP هرچند خطرناک و بیرحم، با تلاشهای مشترک جامعه پزشکی و بیماران، قابل کنترل و درمان است. هر بیمار، یک قهرمان در این میدان نبرد است که با آگاهی، امید و اراده، میتواند بر این بیماری غلبه کند و به زندگی سالم و پرنشاط خود بازگردد.
فراخوان به اقدام
ما شما را دعوت میکنیم تا با گسترش آگاهی درباره TTP و حمایت از تحقیقات پزشکی، به این نبرد بپیوندید. با هم، میتوانیم این بیماری را شکست دهیم و امید را به زندگی هزاران نفر بازگردانیم. بیایید تا با آگاهی و عمل، پیروزی را در این میدان نبرد به ارمغان بیاوریم.